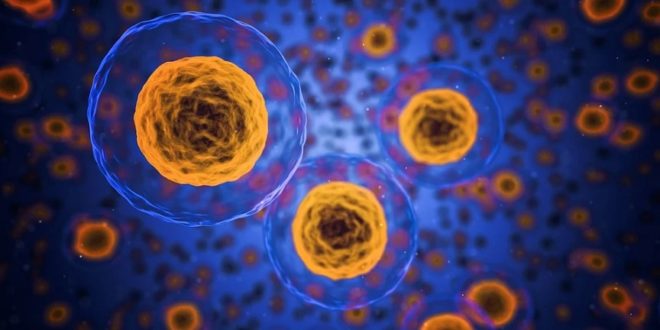
Vědci z Johns Hopkins Medicine tvrdí, že podle nové studie na myších a lidských buňkách vyvinuli umělou lymfatickou uzlinu s potenciálem pro léčbu rakoviny. Tato uzlina – váček naplněný složkami imunitního systému – se implantuje pod kůži a je navržena tak, aby fungovala jako učící se centrum a stimulátor, který dále učí T-buňky (lymfocyty T) imunitního systému rozpoznávat a zabíjet rakovinné buňky.
„Lymfatické uzliny jsou místem, kde T-buňky leží v klidovém stavu a čekají na aktivaci v boji proti infekcím nebo jiným abnormálním buňkám,“ říká spoluautorka studie Natalie Livingston. „Protože rakovina může T-buňky oklamat a nechat je v klidovém stavu, byla umělá lymfatická uzlina navržena tak, aby informovala a aktivovala T-buňky, které jsou vstřikovány vedle lymfatické uzliny.“
K vytvoření umělé lymfatické uzliny vědci použili kyselinu hyaluronovou, zvlhčující látku, která se běžně používá v kosmetice a pleťových krémech a přirozeně se nachází v kůži a kloubech. Díky svým vlastnostem je kyselina hyaluronová častou složkou biologicky odbouratelných materiálů, jako jsou náplasti na hojení ran určené k implantaci nebo aplikaci na tělo. Mezi tyto vlastnosti patří i to, že se kyselina hyaluronová může spojit s T-buňkami prostřednictvím povrchového buněčného receptoru.
Vědci z Johns Hopkins University (hlavní autor Jonathan Schneck) publikovali v roce 2019 výzkum, který ukázal, že kyselina hyaluronová zvyšuje aktivaci T-buněk.
Pro aktuální studii použil tým z Johns Hopkins University kyselinu hyaluronovou jako lešení pro svou novou lymfatickou uzlinu a přidal k ní molekuly MHC (major histocompatibility complex) nebo HLA (human histocompatibility antigen), které aktivují T-buňky a další složky imunitního systému. Dále přidali molekuly a antigeny společné pro rakovinné buňky, aby „naučili“ T-buňky, co mají hledat.
Výsledná umělá lymfatická uzlina má velikost asi 150 mikronů. Je dostatečně malá na to, aby zůstala pod kůží, a naopak dost velká na to, aby nebyla odplavena krevním oběhem.
Výhodou tohoto přístupu oproti jiným buněčným terapiím, jako je CAR-T, má být méně „výrobních“ kroků. Současné buněčné terapie vyžadují odebrání T-buněk pacientovi, jejich manipulaci mimo tělo, aby rozpoznaly určitý typ rakoviny, a jejich vstříknutí zpět pacientovi. „V našem přístupu vstřikujeme T-buňky spolu s umělou lymfatickou uzlinou a T-buňky jsou připravovány a „učeny“ umělou lymfatickou uzlinou uvnitř těla,“ uvádí průvodní tisková zpráva.
Jak se dále praví, metoda umělých lymfatických uzlin se liší od vakcíny proti rakovině, která obvykle aktivuje dendritickou buňku, součást imunitního systému, která učí T-buňky, co mají hledat. U lidí s rakovinou se často objevují špatně fungující dendritické buňky a umělá lymfatická uzlina dendritickou buňku vynechává a aktivuje T-buňky přímo.
Natalie K. Livingston et al, In Vivo Stimulation of Therapeutic Antigen‐Specific T Cells in an Artificial Lymph Node Matrix, Advanced Materials (2024). DOI: 10.1002/adma.202310043
Zdroj: Johns Hopkins University School of Medicine / Phys.org
 Sciencemag.cz
Sciencemag.cz